Por que a textura da carne cultivada depende de scaffolds biomiméticos
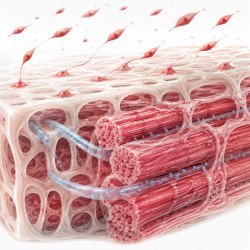
Células musculares isoladas em suspensão não formam fibras. Sem um suporte físico que oriente seu comportamento, elas proliferam de forma desorganizada, produzindo uma massa celular sem estrutura hierárquica reconhecível – nada que se aproxime da textura de um bife ou de um filé.
Um scaffold, no contexto da carne cultivada, é uma matriz tridimensional que substitui o papel do tecido conjuntivo natural, oferecendo superfícies de adesão, orientação espacial e estímulos mecânicos às células. Suas propriedades determinam diretamente atributos sensoriais: a porosidade controla a difusão de nutrientes e influencia a suculência; a topografia superficial guia o alinhamento das miofibras, gerando fibrosidade; a rigidez mecânica afeta a diferenciação celular e a firmeza do produto final.
Materiais com stiffness entre 8 e 17 kPa, por exemplo, favorecem a diferenciação miogênica em células satélite bovinas. A degradação controlada do scaffold permite que a matriz extracelular depositada pelas próprias células vá progressivamente substituindo o suporte sintético, aproximando o produto de um corte inteiro com elasticidade e mordida coerentes.
Materiais e técnicas de fabricação moldam estrutura, custo e comestibilidade
Entre os biomateriais naturais mais estudados, colágeno e gelatina lideram pela excelente biocompatibilidade e adesão celular, além de serem componentes nativos da matriz extracelular muscular. O alginato, derivado de algas, oferece boa estabilidade estrutural e custo acessível, embora sua adesão celular seja fraca sem modificações químicas. A celulose e a quitosana, de origem vegetal e fúngica respectivamente, são promissoras por sua abundância e segurança regulatória, mas podem deixar sabor residual perceptível dependendo do processamento.
Estruturas miceliais de fungos ganharam atenção por formarem redes fibrosas naturalmente porosas, com propriedades mecânicas ajustáveis. Materiais sintéticos como PLGA aparecem em pesquisa, mas a viabilidade para consumo humano permanece incerta.
Quanto às técnicas, o electrospinning produz fibras nanométricas alinhadas que imitam feixes musculares, enquanto o bioprinting permite geometrias tridimensionais precisas. A liofilização gera estruturas porosas uniformes, e scaffolds de plantas descelularizadas, como espinafre, preservam arquitetura vascular que facilita nutrição celular em tecidos mais espessos. Cada método influencia diretamente a textura final do produto.
O desafio real é integrar desempenho biológico e manufatura em escala

Produzir scaffolds que funcionem bem em laboratório é uma coisa. Fazê-los operar dentro de biorreatores industriais, com consistência lote a lote, custo controlado e aprovação regulatória, é um problema de outra ordem de grandeza.
Materiais como proteínas da matriz extracelular oferecem excelente adesão e diferenciação celular, mas são caros e difíceis de produzir em volume. Estruturas densas favorecem textura firme, porém comprometem a difusão de oxigênio e nutrientes para as camadas internas. Bioprinting de alta resolução gera geometrias biomimético precisas, mas o throughput ainda é incompatível com escala alimentar.
A cocultura entre células musculares, adiposas e de tecido conjuntivo adiciona realismo sensorial, mas exige controle fino de microambientes distintos dentro do mesmo sistema. Padronização entre lotes, segurança alimentar e formulação final são obstáculos concretos que a indústria ainda está aprendendo a endereçar, tema recorrente em estudos de Pesquisa de Carne.
Direções promissoras incluem scaffolds comestíveis e biodegradáveis, sistemas híbridos com microcarriers em suspensão, e desenho orientado por dados combinando engenharia de tecidos com ciência de alimentos. Não existe solução única, e talvez não exista.
Sem scaffold eficaz, a textura continua incompleta
Transformar biomassa celular em algo que realmente pareça e se comporte como carne exige mais do que proliferação celular bem-sucedida. O scaffold é o elemento que converte crescimento biológico em organização tecidual reconhecível, influenciando diretamente a firmeza, a mastigabilidade e a coesão do produto final. Seu papel vai além de suporte estrutural: a arquitetura do material orienta a diferenciação celular, distribui tensões mecânicas e determina como fibras musculares se alinham. Materiais comestíveis como proteínas de soja texturizada ou géis de metilcelulose mostram viabilidade em escala, mas ainda enfrentam limitações na fidelidade biomimética. Cortes inteiros, com sua complexidade de camadas e gradientes de textura, permanecem o desafio mais distante. Chegar lá dependerá da convergência entre escolha de materiais, métodos de fabricação como bioimpressão ou eletrofiação, e engenharia de biorreatores capazes de sustentar esse processo com viabilidade econômica real.